Überblick | Prinzip | Indikation | Probennahme | Leistung | Ihr Vorteil | Literatur | Verfügbarkeit

In aller Kürze
- Epigenetischer DNA-Methylierungstest zur Detektierung aller Karzinome, die vom Uterus ausgehen, insbesondere Endometriumkarzinom, aber auch endozervikales Karzinom.
- Der Test ist indiziert bei peri- und postmenopausalen Frauen mit abnormalen vaginalen Blutungen.
- Probenentnahme durch Zervikovaginalabstrich.
- 95 % weniger falsch-positive Ergebnisse, verglichen mit transvaginalem Ultraschall.
- Die Anwendung reduziert die Anzahl der Frauen, die sich einer Hysteroskopie mit Kürettage unterziehen müssen um 90 %.
- Ein negatives WID®-easy Testergebnis deutet mit hoher Wahrscheinlichkeit darauf hin, dass keine Malignität vorliegt, so dass die konservative Behandlung und die aktive Überwachung für viele Patienten eine Alternative zur Krankenhausüberweisung darstellen.
Das Prinzip des WID®-easy Tests
Indikation
Test zur einfachen und schnellen Abklärung von Frauen, die mit Symptomen vorstellig werden, die auf ein Endometriumkarzinom hinweisen. Hierbei handelt es sich insbesondere um peri- und postmenopausale Frauen mit abnormalen vaginalen Blutungen.
Der Ablauf
Ein Zervikovaginalabstrich wird an das diagnostische Labor gesendet.
Nach DNA Extraktion und Bisulfitkonvertierung wird eine quantitative PCR-Reaktion durchgeführt.
Der WID®-easy Test, der in der Fachliteratur als „WID-qEC Test“ bezeichnet wird, misst den Methylierungsstatus von DNA-Regionen der Gene GYPC und ZSCAN12, von denen bekannt ist, dass sie bei Endometriumkarzinom und Zervixkarzinom sehr stark methyliert sind.
Diese Messwerte (angegeben in „PMR“ = „Percentage of fully Methylated Reference“) werden summiert und ergeben „∑ PMR“. Das Resultat des Tests hängt von dem ermittelten Wert ∑ PMR ab und wird im Testbericht an den/die ÄrztIn übermittelt.
Quellen: www.eutops.at und Evans et al., The Lancet Oncology, 2023
Das Testergebnis
Das Testergebnis liegt Ihnen in wenigen Tagen vor. Bitte fragen Sie bei Ihrem Labor nach den aktuellen Bearbeitungszeiten (Proben Eingang im Labor bis zur Ausgabe des Befundberichts) für den WID®-easy Test.
Der Befundbericht gibt den ermittelten ∑PMR-Wert an, sowie eine Interpretation des Ergebnisses in Anlehnung an Evans et al., 2023. Die Formulierung des Testergebnises liegt in der Verantwortung der Gesundheitseinrichtung, die den Test herstellt und verwendet.
Die Probenahme*
Die Probenahme erfolgt unter Verwendung von Copan-Swab und Medium.

Copan-Swab und Medium
Die Probenahme erfolgt unter Verwendung des Copan FLOQswab™ (552C.80PB) und des eNAT Mediums (608C) der Firma Copan, welche auch ein entsprechendes Kit anbietet (608CS01R). Beides wird Ihnen von Ihrem Labor zur Verfügung gestellt.
Das Vorgehen
Vor der Probenahme für den WID®-easy Test soll kein Gleitmittel verwendet werden.
Die Probenahme für den WID®-easy Test erfolgt
- vor der Probenahme für einen anderen Test, z. B. für einen PAP-Abstrich.
- vor dem Einbringen einer anderen Substanz in die Vagina oder in die Nähe des Gebärmutterhalses, z. B. Essigsäure zur visuellen Inspektion (VIA).
- vor dem transvaginale Ultraschall
- oder frühstens drei Tage nach diesen Maßnahmen.
Eine detaillierte Anleitung zur Probenahme kann unter folgendem Link abgerufen werden.*
Einschränkungen
Der WID®-easy Test weist die für Endometriumkrebs typischen Methylierungsmuster der Tumor-DNA nach.
Bedingungen, die den Abfluss von Tumor-DNA aus der Gebärmutterhöhle in die Vagina einschränken, z. B. große endozervikale Polypen oder Myome, können die Empfindlichkeit des Tests beeinträchtigen.
Die Patientin soll mindestens die letzten 24 Stunden vor der Abnahme des WID®-easy Tests keinen vaginalen Geschlechtsverkehr ohne die Verwendung von Kondomen haben.
* Die konkrete Anleitung zur Probenahme liegt in der Verantwortung der Gesundheitseinrichtung, die den Test herstellt und verwendet. Diese wird ihnen von der Gesundheitseinrichtung zur Verfügung gestellt. Bei dem hier dargestellten Muster handelt es sich um eine aktuelle Arbeitshypothese.
S3-Leitlinie Endometriumkarzinom
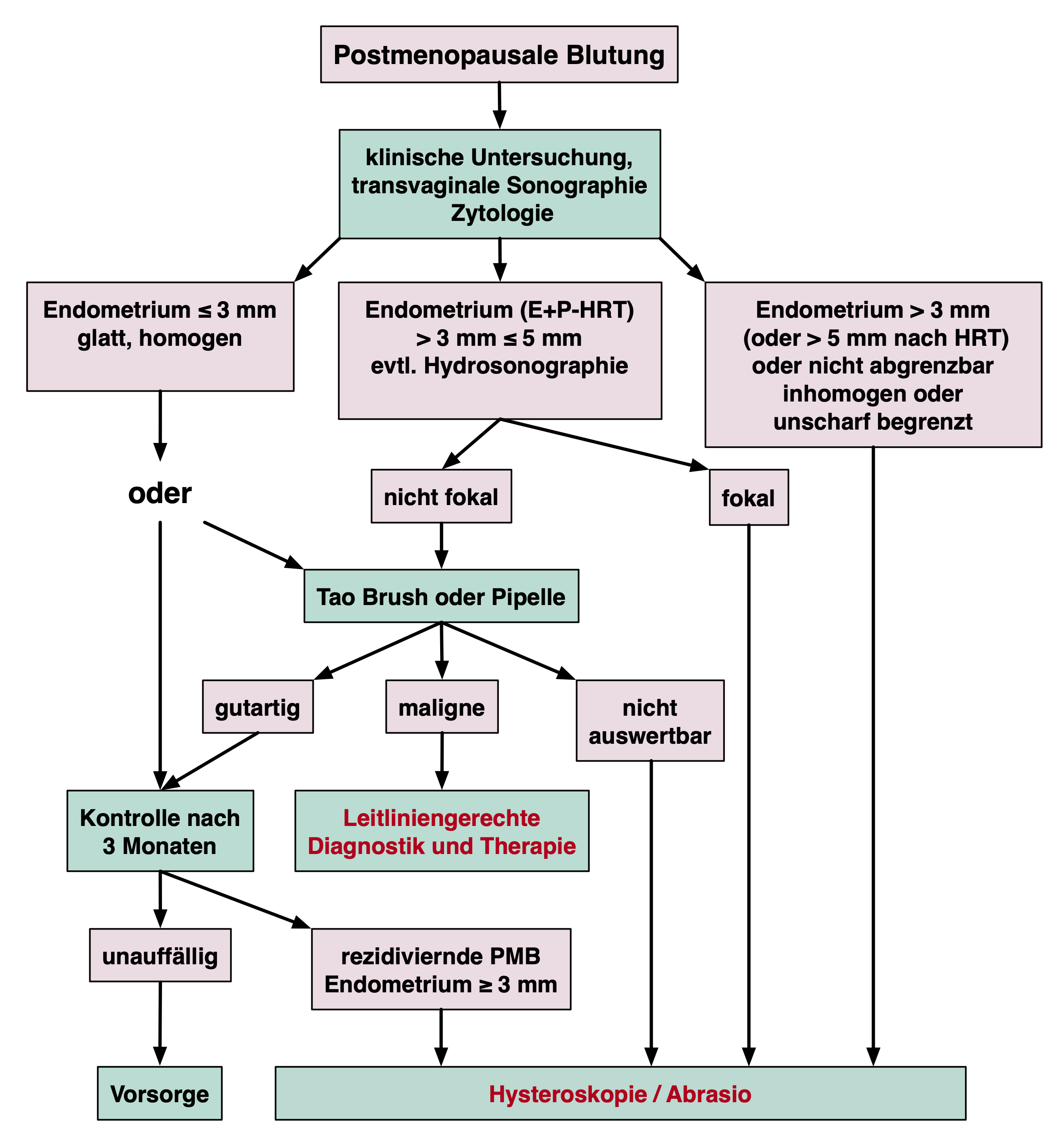
Diagnostischer Pfad für Patientinnen mit postmenopausalen Blutungen
Entsprechend den S3-Leitlinie Endometriumkarzinom AWMF-Registernummer: 032/034-OL von September 2022 wird nach klinischer Untersuchung zunächst ein transvaginaler Ultraschall, sowie eine zytologische Untersuchung empfohlen.
Der transvaginale Ultraschall bestimmt die Endometriumsdicke und bei einer Dicke von ≥ 3 mm werden operative diagnostische Verfahren, wie Tao Brush™, Pipelle™, Hysteroskopie und Kürettage empfohlen.
Bei Frauen mit peri- und postmenopausalen abnormalen Blutungen ist dieser Grenzwert in über 50 % der Fälle erreicht oder überschritten.
(Evans et al., The Lancet Oncology, 2023).
Die Leistung des WID®-easy Tests im Vergleich zur transvaginalen Ultraschalluntersuchung
Die Leistung des WID®-easy Tests im Vergleich zur transvaginalen Ultraschall-untersuchung
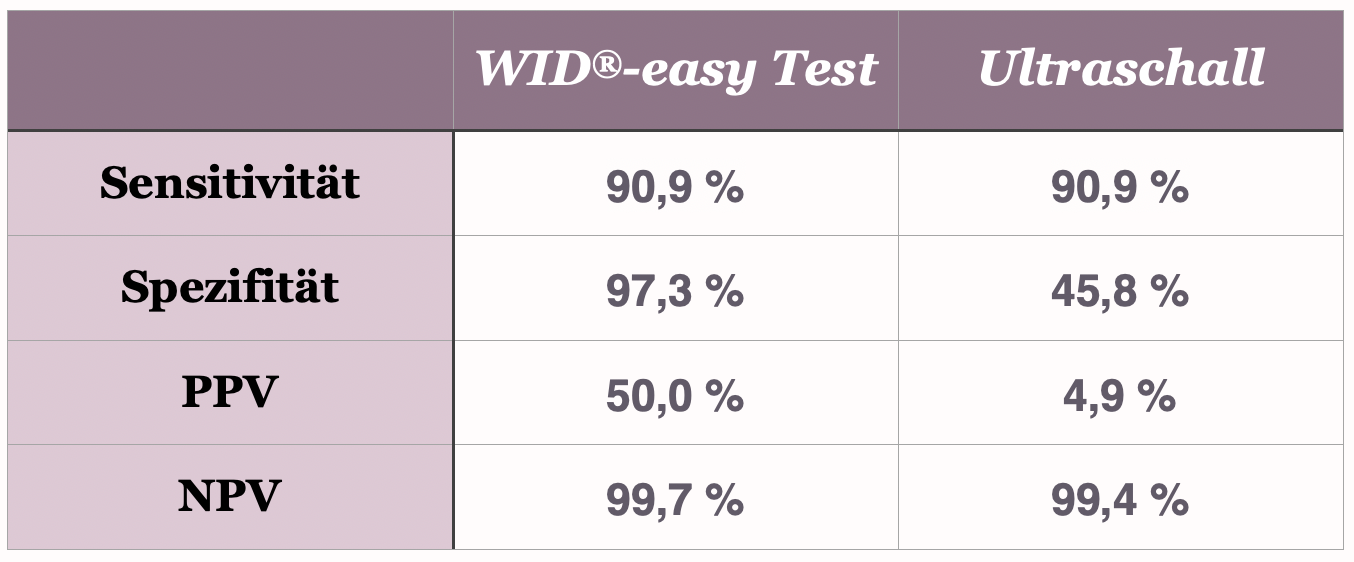
Der WID®-easy Test zeichnet sich durch extrem hohe Werte für die Sensitivität (90,9 %), Spezifität (97,3 %) und den NPV (99,7 %) aus.
Unter Verwendung des ∑PMR cut-off-Werts von 0,3 ist der PPV des WID®-easy Tests mit 50 % zehnmal höher als der der Sonographie, deren PPV nur 5 % beträgt.
(Evans et al., The Lancet Oncology, 2023)
90 % weniger operative diagnostische Eingriffe
Über 50% falsch Positive
beim Ultraschall
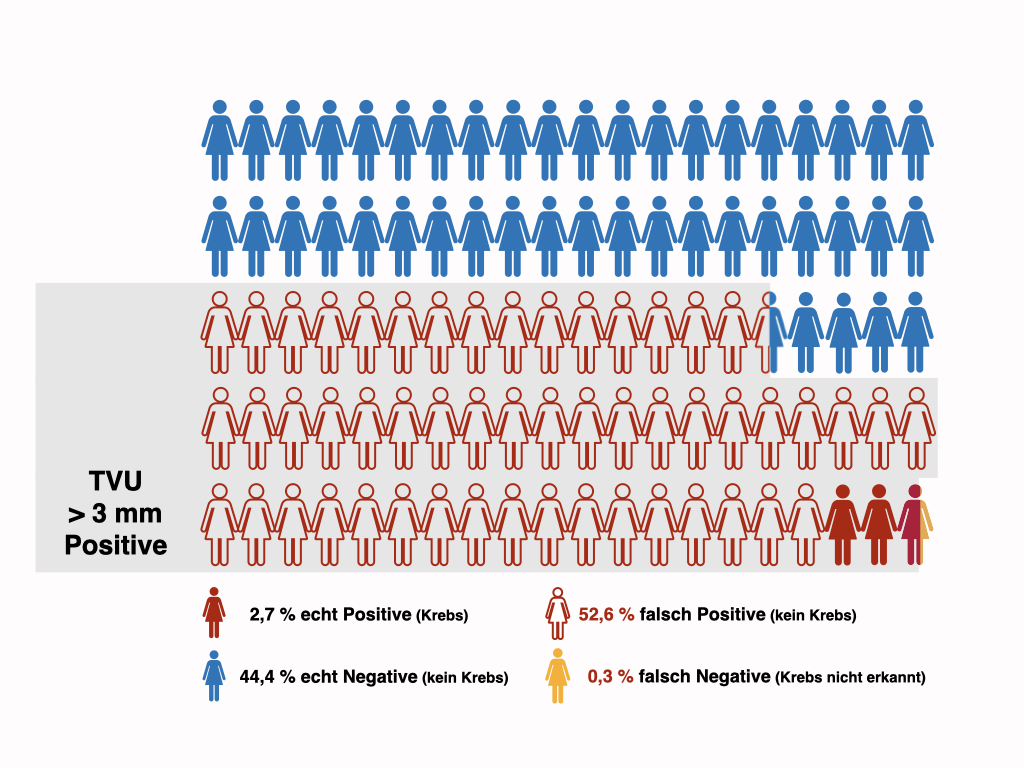
Die grau unterlegte Fläche zeigt den Anteil (> 55 %) der Frauen mit peri- oder postmenopausalen Blutungen an, die sich aufgrund der Bestimmung der Endometriumsdicke mittels transvaginalem Ultraschall einem operativen diagnostischen Verfahren unterziehen müssen, obwohl bei nichtmals 3 % dieser Frauen Krebs vorliegt. Das ist eine Rate falsch positiver Ergebnisse von über 50 %.
Keine 3 % falsch Positive
bei WID®-easy Test
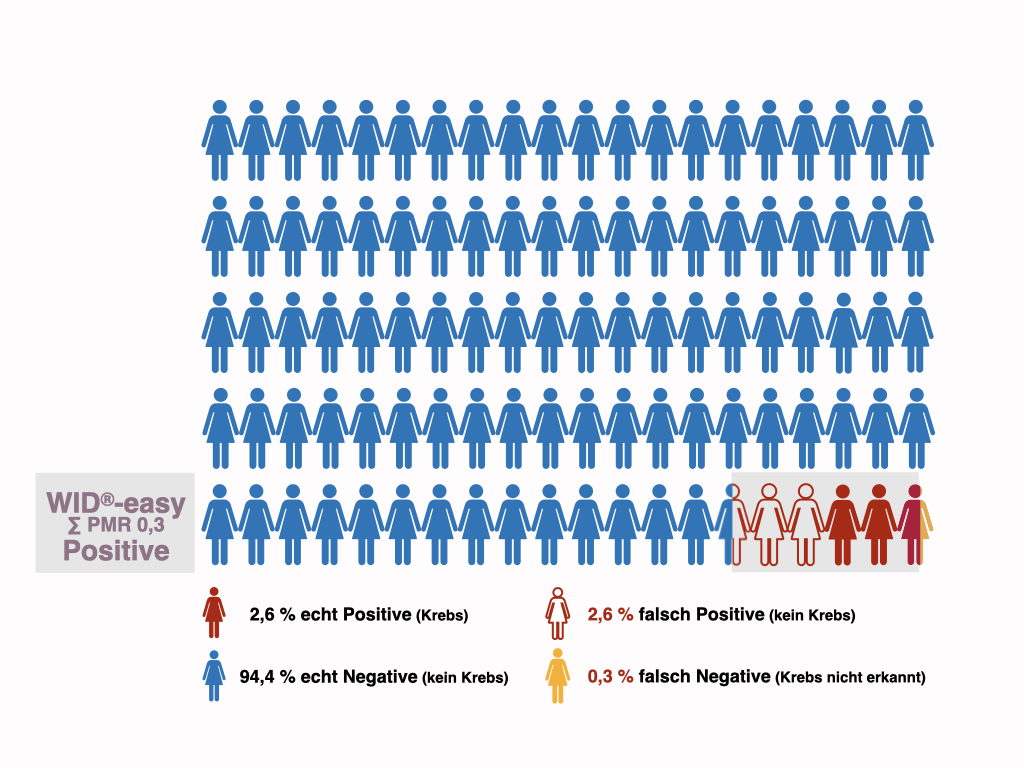
Der Anteil (5,2 %) der Frauen mit peri- oder postmenopausalen Blutungen, die sich aufgrund eines positiven WID®-easy Testergebnisses einem operativen diagnostischen Verfahren unterziehen müssen, ist hier grau unterlegt dargestellt. Der Anteil falsch positiver Ergebnisse liegt dabei unter 3 %. Das ist eine Reduktion der falsch Positiven um 95%.
Extrapoliert auf 100 peri- und postmenopausale Frauen, die sich mit abnormalen Blutungen vorstellen, wird bei der transvaginalen Ultraschalluntersuchung („TVU“) der Grenzwert von 3 mm für die Endometriumsdicke bei 55 Frauen überschritten werden. Entsprechend den S3-Leitlinien müssen all diese Frauen einer operativen diagnostischen Abklärung (Tao Brush™, Pipelle™, Hysteroskopie oder Kürettage) unterzogen werden. Bei über 50 dieser Frauen wird sich herausstellen, dass kein Endometrium- oder Zervixkarzinom vorliegt. Es lag somit ein falsch positives Ergebnis vor.
Aufgrund der höheren Spezifität des WID®-easy Tests (97,3 % WID®-easy / 45,8 % TVU), die zu einem deutlich höheren positiven Vorhersagewert gegenüber dem transvaginalen Ultraschall führt (PPV 50,0 % WID®-easy / 4,9 % TVU), schlägt der WID®-easy Test nur bei fünf Frauen eine invasive Abklärung vor. Das ist eine Reduktion invasiver Eingriffe um 90 %. Und bei der Hälfte dieser Frauen wird in der histologischen Untersuchung auch Krebs diagnostiziert werden.
Die Rate der falsch positiven Ergebnisse ist beim Ultraschall um das Zwanzigfache höher als beim WID®-easy Test (52,6 % gegenüber 2,6 %). Durch die Nutzung des WID®-easy Tests können daher 95 % der invasiven diagnostischen Eingriffe bei Frauen vermieden werden, bei denen sich letztendlich herausstellt, dass sie nicht an einem Endometriumkarzinom leiden.
Dabei sind Sensitivität, der negative Vorhersagewert (NPV) und die Rate falsch negativer Ergebnisse bei beiden Methoden vergleichbar.
(Evans et al., The Lancet Oncology, 2023)
Robustheit und Komplikationen
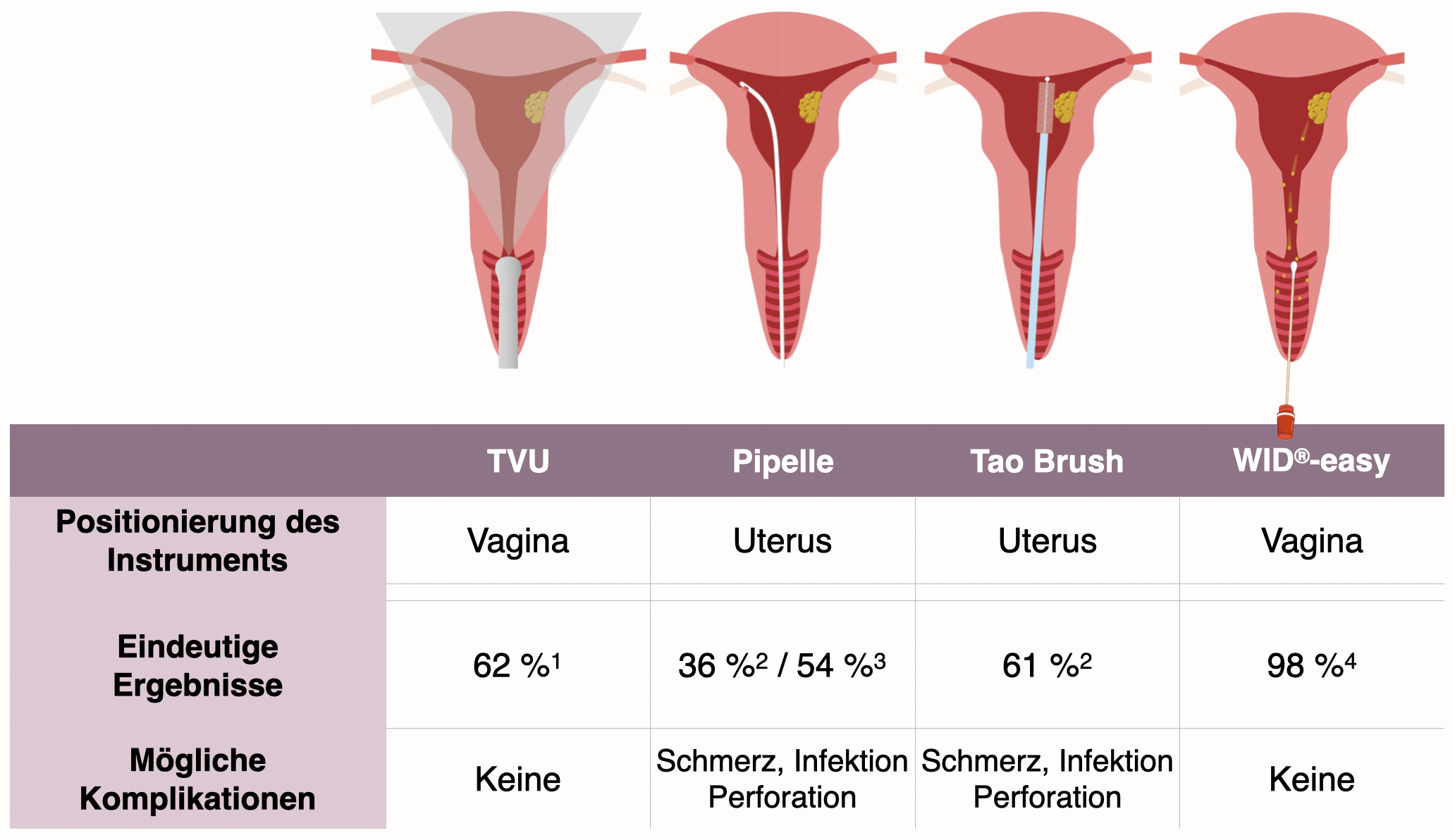
WID®-easy Test im Vergleich zu TVU, Pipelle und Tao Brush
Im Gegensatz zu den Untersuchungen mittels transvaginalem Ultraschall, Pipelle™ oder Tao Brush™, führt die Durchführung des WID®-easy Tests fast immer (98 %) zu einem eindeutigen Ergebnis und es sind keine Komplikationen zu erwarten.
Neben der überzeugenden Leistung des WID®-easy Tests (Sensitivität, Spezifität, NPV, PPV) zeichnet sich der Test auch durch eine überragende Robustheit aus. Darüberhinaus kann davon ausgegangen werden, dass der Test zu keinen Komplikationen führen wird.
In fast 40 % der Fälle muss beim transvaginalen Ultraschall und beim Tao Brush™ damit gerechnet werden, kein schlüssiges Ergebnis zu bekommen. Bei der Untersuchung mittels Pipelle™ liegt der Erwartungswert für den Anteil eindeutiger Ergebnisse eher unter 50 %.
Die Durchführung des WID®-easy Tests hingegen führt fast immer zu einem eindeutigen Ergebnis (98 %).
Die Untersuchungen mittels Pipelle™ und Tao Brush™ erfordern das Einbringen der Instrumente durch den zervikalen Kanal in den Uterus. Hierbei kann es zu Schmerzen oder Infektionen kommen und in manchen Fällen sogar zur Uterusperforation.
Endozervikales Karzinom
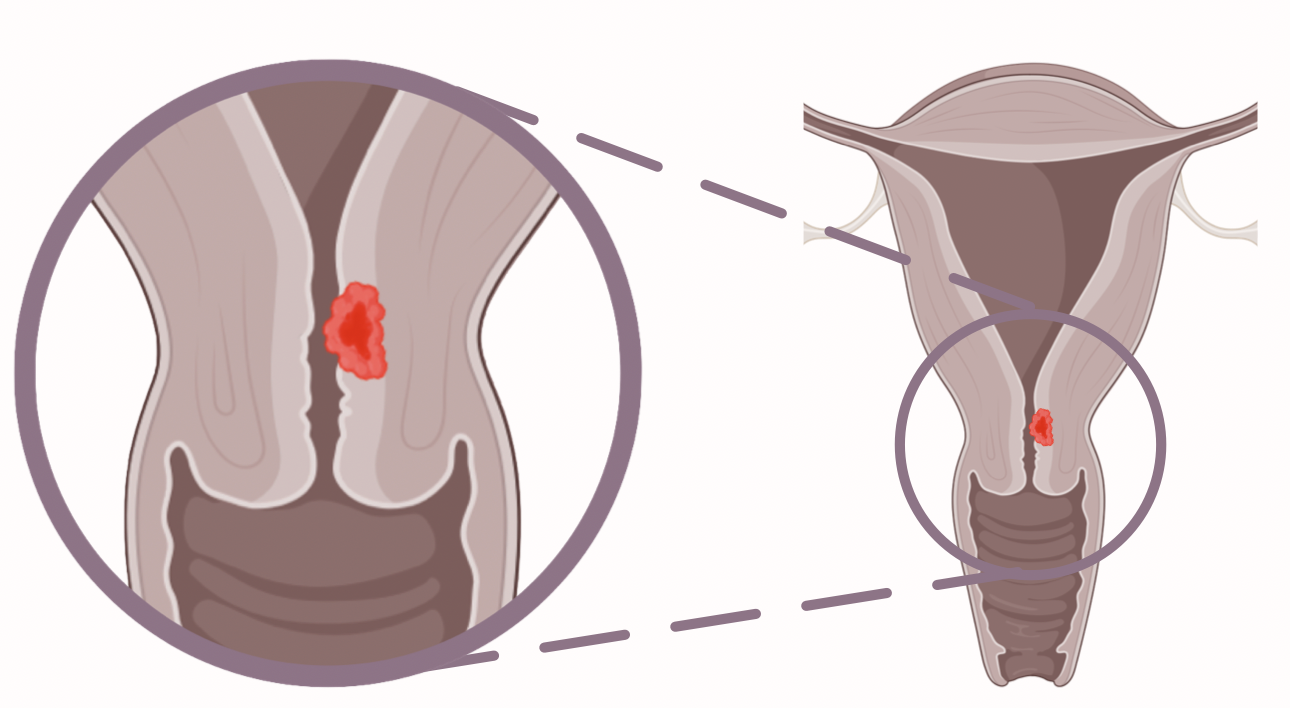
Das endozervikale Karzinom
Endozervikale Karzinome sind nicht im Rahmen der visuellen Inspektion mittels Spekulum zu erkennen. Darüber hinaus führen diese nicht zu einer erhöhten Endometriumsdicke und bleiben auch in der Zytologie unauffällig.
In einer Case-Control Studie hat der WID®-easy Test von 22 Cervixkarzinomen 21 erkannt und somit eine Sensitivität von 95 %
(Schreiberhuber et al., International Journal of Cancer, 2022).
Mehr konservative Behandlungen
Bei Verdacht auf Endometriumkarzinom ist eine rasche Abklärung entscheidend, um die Überlebenschancen zu maximieren, falls tatsächlich ein Endometriumkarzinom vorliegt (Sud et al., The Lancet Oncology, 2020).
Im Falle eines negativen WID®-easy Tests ist die konservative Behandlung von Frauen mit abnormalen Blutungen und die aktive Überwachung mit transvaginalem Ultraschall und dem WID®-easy Test eine echte Option.
Sie ersparen Ihrer Patientin einen chirurgischen Eingriff im Krankenhaus und bleiben während der konservativen Behandlung in engem Kontakt mit Ihrer Patientin als deren primäre(r) AnsprechpartnerIn.

Wissenschaftliche Publikationen zum WID®-easy Test
Evans et al. (2023)
Evans, I., Reisel, D., Jones, A., Bajrami, A., Nijjar, S., Solangon, S. A., Arora, R., Redl, E., Schreiberhuber, L., Ishaq-Parveen, I., Rothärmel, J., Herzog, C., Jurkovic, D. & Widschwendter, M. (2023). Performance of the WID-qEC test versus sonography to detect uterine cancers in women with abnormal uterine bleeding (EPI-SURE): a prospective, consecutive observational cohort study in the UK. The Lancet Oncology, 24(12), 1375–1386. https://doi.org/10.1016/s1470-2045(23)00466-7
Real-Life Vergleich zum Stand der Technik
In einer prospektiven Studie wurde die Leistung der aktuellen verbesserten Ausführung des WID-qEC Tests mit dem Standardverfahren im Vereinigten Königreich verglichen. Die Studie fand am UCL-Hospital in London statt.
400 Frauen im Alter ab 45 Jahren mit peri- oder postmenopausalen abnormalen Blutungen nahmen an der Studie teil.
Der WID-qEC Test reduziert die Zahl der Frauen, die chirurgische Diagnoseverfahren wie Hysteroskopie und Kürettage benötigen, obwohl sie keinen Krebs haben, um 87 % im Vergleich zum Standardverfahren in Großbritannien und um 95 % im Vergleich zum Standardverfahren in Deutschland, der Schweiz und Österreich.
Der WID-qEC Test beschleunigt die Diagnose bei Frauen mit Symptomen von Endometriumkrebs, was zu besseren Ergebnissen und Kosteneinsparungen im Gesundheitswesen führt.
Herzog et al. (2022)
Herzog, C., Marín, F., Jones, A., Evans, I., Reisel, D., Redl, E., Schreiberhuber, L., Paytubi, S., Pelegrina, B., Carmona, Á., Peremiquel-Trillas, P., Frias-Gomez, J., Pineda, M., Brunet, J., Ponce, J., Matias-Guiu, X., De Sanjosé, S., Alemany, L., Olaitan, A., . . . Widschwendter, M. (2022). A Simple Cervicovaginal Epigenetic Test for Screening and Rapid Triage of Women With Suspected Endometrial Cancer: Validation in Several Cohort and Case/Control Sets. Journal Of Clinical Oncology, 40(33), 3828–3838. https://doi.org/10.1200/jco.22.00266
Entwicklung und Validierung in fünf verschiedenen Settings
Diese Veröffentlichung beschreibt die Entwicklung und Validierung des WID-qEC Tests.
Der Test wurde anhand von 726 zervikovaginalen Abstrichen von Frauen mit und ohne Endometriumkarzinom entwickelt und in 562 davon unabhängigen zervikovaginalen Proben unter Verwendung von drei verschiedenen Entnahmemethoden und zwei diagnostischen sowie zwei prädiktiven Settings validiert.
Schreiberhuber et al. (2022)
Schreiberhuber, L., Herzog, C., Vavourakis, C. D., Redl, E., Kastner, C., Jones, A., Evans, I., Zikan, M., Cibula, D., Widschwendter, P., Pfau, K., Math, B., Seewald, M., Amory, S., Obrist, P. & Widschwendter, M. (2022). The WID‐qEC test: Performance in a hospital‐based cohort and feasibility to detect endometrial and cervical cancers. International Journal Of Cancer, 152(6), 1269–1274. https://doi.org/10.1002/ijc.34275
Real-Life Kohorte und Validierung für Gebärmutterhalskrebs
WID-qEC Test wurde in einer real-Life Krankenhauskohorte von 304 Frauen validiert.
Darüber hinaus wurde in einer Case-Control-Studie die Überlegenheit des WID-qEC Test in der Detektion von Zervixkarzinom, v.a. endozervikaler Karzinome, gegenüber der zytologischen Untersuchung gezeigt.
Redl et al. (2024)
Redl, E., Schreiberhuber, L., Ishaq, I., & Widschwendter, M. (2024). High-throughput implementation of the WID-qEC Test: DNA methylation-based test for the detection of uterine cancers. Wiley Analytical Science.
Entwicklung der Hochdurchsatzanalytik
Der Artikel beschreibt die technische Umsetzung und die analytische Verifizierung des WID-qEC-Tests.
Der beschriebene Arbeitsablauf umfasst nicht nur die qPCR-Analyse selbst, sondern auch den gesamten Testprozess, einschließlich der Probenentnahme, der automatisierten DNA-Isolierung, Quantifizierung und Normalisierung und der automatisierten Bisulfit-Konvertierung sowie der nachgeschalteten Analyse und Dateninterpretation.
Dieser Prozess ermöglicht es den Labors, eine große Anzahl von Proben außergewöhnlich effizient zu verarbeiten.
Illah et al. (2024)
Illah, O., Scott, M., Redl, E., Barrett, J. E., Schreiberhuber, L., Herzog, C., Vavourakis, C. D., Jones, A., Evans, I., Reisel, D., Chandrasekaran, D., Doufekas, K., Graham, R., Kotsopoulos, I. C., MacDonald, N., Arora, R., Olaitan, A., Rosenthal, A. & Widschwendter, M. (2024). High performance of the DNA methylation‐based WID‐qEC test for detecting uterine cancers independent of sampling modalities. International Journal Of Cancer, 155(5), 800–806. https://doi.org/10.1002/ijc.35000
Vergleich verschiedener Probenentnahmeverfahren
In der Studie wurde untersucht, ob unterschiedliche Probenentnahmeverfahren die Validität des Tests beeinflussen. Konkret wurden die Cervex-Bürste und PreservCyt mit dem FLOQSwab und eNAT, die von ÄrztInnen durchgeführte Probenentnahme mit der Selbstentnahme durch Patientinnen und unterschiedliche Entnahmestellen (vaginal, zerviko-vaginal oder zervikal) verglichen, um etwaigen Einfluss auf die Leistungsfähigkeit des Tests zu bewerten.
Die Ergebnisse zeigten, dass die Testeresultate unabhängig von der Entnahmemethode konstant blieben, selbst bei Proben, die sieben Tage lang bei Raumtemperatur gelagert wurden. Während die Selbstentnahme zu einer hohen Spezifität führte, war die Sensitivität etwas geringer.
Insgesamt bietet der WID-qEC-Test eine einfache, objektive und nicht-invasive Methode zur Bewertung des Malignitätsrisikos bei Frauen mit abnormen Blutungen.
Ken-Amoah et al. (2024)
Ken‐Amoah, S., Redl, E., Domson, B. K. S., Barrett, J. E., Schreiberhuber, L., Herzog, C., Arora, R., Jones, A., Evans, I., Reisel, D., Lamptey‐Mills, E., Nachinab, V. B., Pepera, T., Olaitan, A., Obiri‐Yeboah, D., Akakpo, P. K. & Widschwendter, M. (2024). Performance of the WID‐qEC test to detect uterine cancers in black women with abnormal uterine bleeding: A prospective observational cohort study in Ghana. International Journal Of Cancer, 156(5), 1055–1064. https://doi.org/10.1002/ijc.35260
Die Leistung des WID-qEC-Tests zur Detektion von Gebärmutterkrebs bei schwarzen Frauen mit abnormalen Blutungen
Die Autoren untersuchten die Leistung des WID-qEC Tests, Gebärmutterkörper- und Gebärmutterhalskrebs bei schwarzen Frauen in Ghana zu erkennen, die mit abnormalen Blutungen vorstellig wurden.
Mit dem WID-qEC Test konnten 100 % der Endometrium- und Zervixkarzinome in der Studienpopulation erfolgreich identifiziert werden. Durch die einfache Probenentnahme und die kostengünstige PCR-basierte Analyse mit hohem Durchsatz ist der WID-qEC Test ein vielversprechendes Instrument zur Erkennung von Endometriumkrebs bei allen Frauen in Ländern mit niedrigem und mittlerem Einkommen und bei ethnischen Gruppen, bei denen die Leistung des Ultraschall bekanntermaßen besonders schlecht ist.
Redl et al. (2026)
Redl, E., Herzog, C., Vavourakis, C., Barrett, J., Jones, A., Evans, I., Reisel, D., Manchanda, R., Bjørge, L., Zikan, M., Cibula, D., Alkasalias, T., Rådestad, A. F., Gemzell-Danielsson, K., Dubeau, L., MacDonald, N., Jurkovic, D., Pashayan, N. & Widschwendter, M. (2026). The cervico-vaginal DNA methylation WID-qEC test: An epigenetic marker associated with ovarian cancer in the absence of endometrial and cervical cancer. International Journal Of Cancer, 1-7. doi:10.1002/ijc.70354
Zusammenhang zwischen WID®-easy-Positivität und Eierstockkrebs
Die Studie untersuchte die Positivität von WID®-easy (WID-qEC) bei Frauen ohne Gebärmutterhals- oder Endometriumkarzinom. Von 1.269 Proben waren 6,3 % positiv. Eierstockkrebs war der stärkste unabhängige Prädiktor für eine Positivität (adjustierte OR 2,93), und auch eine höhere Anzahl ovulatorischer Zyklen im Laufe des Lebens war unabhängig mit einer Positivität assoziiert.
In einer modellierten symptomatischen Population mit einer Ausgangsprävalenz für Eierstockkrebs von 0,38 % entspricht eine WID-qEC-Positivität einer geschätzten Wahrscheinlichkeit von etwa 1,3 % — ein deutlicher Anstieg gegenüber dem Ausgangswert, auch wenn das absolute Risiko weiterhin niedrig bleibt.
Snowsill et al. (2026)
Snowsill, T. M., Sleigh, S., Barrett, J. & Widschwendter, M. (2026). Cost-Minimization Analysis of the Women’s Cancer Risk Identification—Quantitative Polymerase Chain Reaction Test for Endometrial Cancer Epigenetic Biomarker Compared With Transvaginal Ultrasound for Triaging Abnormal Uterine Bleeding. Value in Health. doi:10.1016/j.jval.2026.03.2235
WID®-easy vs. transvaginaler Ultraschall: Eine Kostenminimierungsanalyse im UK NHS
Eine Kostenminimierungsanalyse im britischen Gesundheitssystem (NHS) verglich den WID®-easy Test (WID-qEC) mit dem transvaginalen Ultraschall (TVUS) als First-Line-Triage-Test bei Frauen ab 45 Jahren mit abnormer uteriner Blutung. Auf Basis eines Entscheidungsbaummodells, gestützt auf die EPI-SURE-Kohorte (n=399) und die NHS Reference Costs 2023/24, benötigten unter der WID®-easy-Strategie nur 12 % der Frauen eine definitive invasive Abklärung – gegenüber 57 % unter der TVUS-Strategie.
Der Break-Even-Preis für Kostenäquivalenz lag bei £302 pro Test. Bei einem indikativen Preis von £200 überstieg die Wahrscheinlichkeit für Kosteneinsparungen 99 %; bei £150 ergaben sich mittlere Einsparungen von £152 pro Patientin. Über BMI- und ethnische Subgruppen hinweg blieben die Break-Even-Preise stabil (£290–£331). Der gewählte Kostenminimierungsansatz misst der Reduktion von Schmerzen, Angst und diagnostischer Verzögerung keinen Wert bei – Effekten, die eine geringere Zahl an Hysteroskopien und Endometriumbiopsien dem überlasteten NHS-System bringen würde, in dem sich die Eilüberweisungen bei Krebsverdacht in den letzten Jahren (2009–2023) mehr als verdreifacht haben.
Olaitan et al. (2026)
Olaitan, A., Pashayan, N., Butler, J., Cibula, D., Costas, L., Crosbie, E. J., Falconer, H., Fotopoulou, C., Akapo, P. K., MacDonald, N., Moss, E., Mueller, M., Rosenthal, A. N., Sundström, K., Hillemanns, P., Manchanda, R., Sleigh, S. & Widschwendter, M. (2026). Transforming Endometrial Cancer Diagnosis: The Case for Molecular Triage in Abnormal Uterine and Postmenopausal Bleeding. International Journal of Gynecological Cancer. doi:10.1016/j.ijgc.2026.104772
Endometriumkarzinom-Diagnostik vor dem Umbruch: Plädoyer für molekulare Triage
Eine internationale Übersichtsarbeit im International Journal of Gynecological Cancer kritisiert den aktuellen Diagnosepfad bei abnormer Uterusblutung. Bei einer Krebsprävalenz von nur 3 % führt der Standardpfad (transvaginaler Ultraschall + Hysteroskopie/Biopsie) zu rund 33 Biopsien pro entdecktem Karzinom, übersieht ~25 % der prognostisch schlechtesten serösen Tumoren und ist bei schwarzen Frauen deutlich schwächer.
Als Alternative wird molekulare Triage diskutiert. Der WID-qEC-Test (WID®-easy) erreichte in der EPI-SURE-Kohorte (n=399) eine Sensitivität von 90,9 %, Spezifität von 92,1 % und einen NPV von 99,7 %. Bei 3.500 jährlichen Überweisungen ließen sich die dringenden Hysteroskopien von 1.850 auf 210 reduzieren – bei Detektion von über 95 % aller Karzinome.
Sie interessieren sich für den WID®-easy Test?
In der Europäischen Union und in der Schweiz wird der WID®-easy Test von Gesundheitseinrichtung, wie z.B. diagnostischen Laboratorien, entsprechend der europäischen In-Vitro-Diagnostik-Verordnung (IVDR) Artikel 5, Absatz 5, oder entsprechenden nationalen Regelungen hergestellt und verwendet.
In Großbritannien erfüllt der WID®-easy Test die Anforderungen der UKCA-Kennzeichnung entsprechend den Vorschriften für Medizinprodukte von 2002 (SI 2002 Nr. 618, in der geänderten Fassung) (UK MDR 2002).
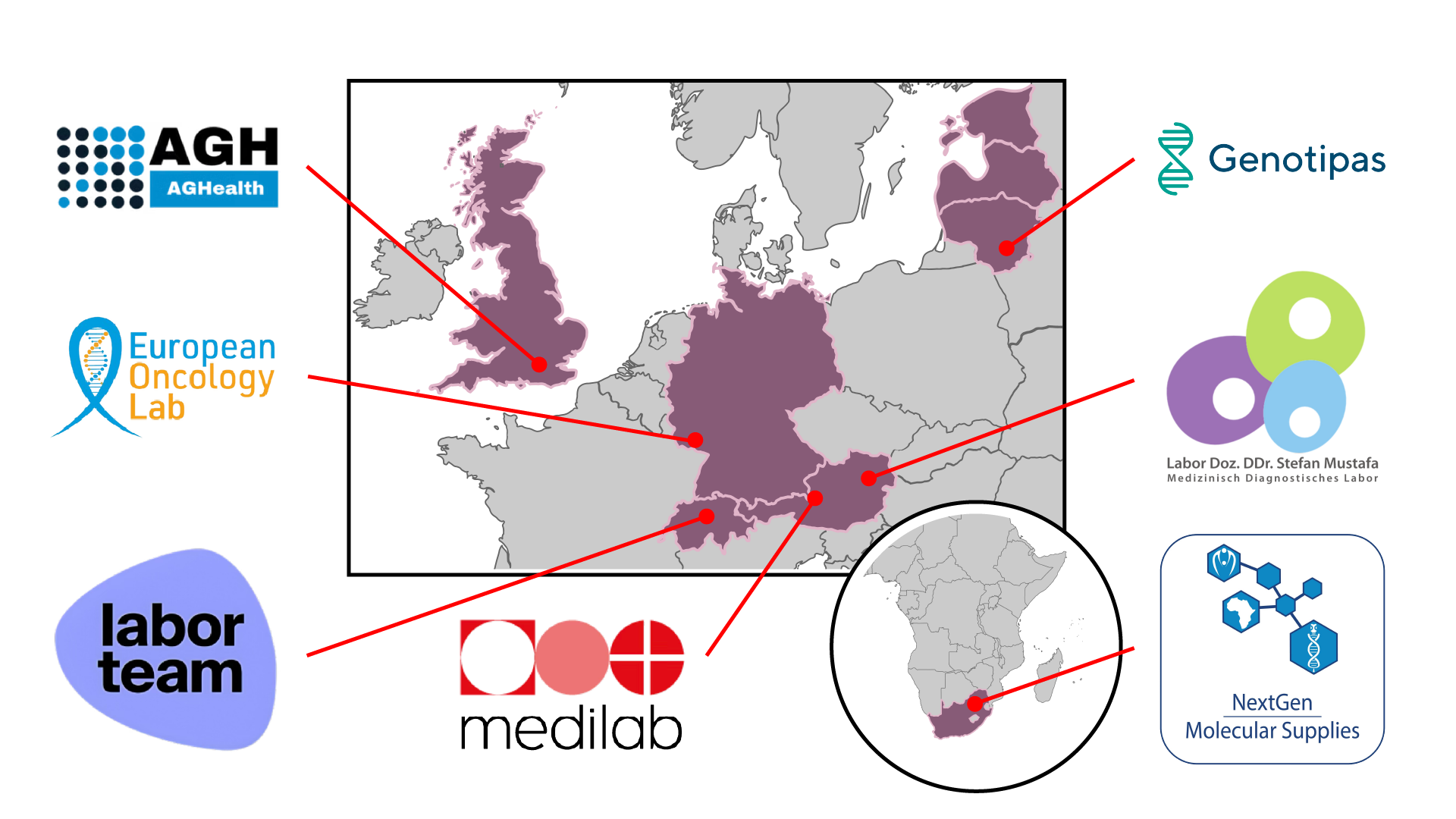
Partner, die den WID®-easy-Test derzeit bereits anbieten, finden Sie auf der unten dargestellten Karte. Bitte wenden Sie sich direkt an einen dieser Anbieter, um die erforderlichen Unterlagen und Materialien für die Beauftragung, Probenahme und Logistik zu erhalten.

Advanced Global Health Ltd
30 Great Guildford Street, London, Großbritannien
Tel: +44 207 078 8867
Mail: info@aghealth.co.uk
Web: www.aghealth.co.uk

European Oncology Lab GmbH
Klaus-Tussing-Str. 2 / Gesundheitspark 2, 66386 St. Ingbert, Deutschland
Tel: +49 6894 95310
Mail: labor@europeanoncologylab.com
Web: www.europeanoncologylab.com

labor team w ag
Blumeneggstrasse 55, 9403 Goldach, Schweiz
Tel: +41 71 844 45 45
Mail: info@team-w.ch
Web: www.laborteam.ch

Labor – Doz. DDr. Stefan Mustafa
Ziehrerplatz 9, 1030 Wien, Österreich
Tel: +43 1 713 91 88
Mail: office@labor-mustafa.at
Web: www.labor-mustafa.at

Medilab GmbH
Strubergasse 20, 5020 Salzburg, Österreich
Tel: +43 662 2205
Mail: office@medilab.at
Web: www.medilab.at

NextGen Molecular Supplies
Incubation Drive 8, 2021 Midrand, Südafrika
Tel: +27 87 148 9309
Mail: customer_care@ngms.co.za
Web: www.ngms.co.za

UAB Genotipas
Aviečių g. 14, 08418, Vilnius, Litauen
Tel: +370 686 55909
Mail: info@genotipas.lt
Web: www.genotipas.lt






